Inleiding
Borstreconstructies zijn de laatste jaren een groot onderdeel geworden in de praktijk van de reconstructieve plastisch chirurg. Dit heeft verschillende oorzaken. Vooreerst is en blijft borstkanker een van de meest voorkomende tumoren bij de vrouw (1 op 10). Door diverse screenings-onderzoeken die via de overheid gepromoot worden en door de bewustwording van de Belgische vrouw dat borstonderzoek op regelmatige wijze dient te gebeuren, worden er meer borsttumoren in een vroeger stadium ontdekt. Hierdoor stijgt het aantal operatieve mogelijkheden waarbij borstchirurgie (al dan niet gecombineerd met een bijkomende behandeling zoals chemo- en/of radiotherapie) voor een definitieve genezing kan zorgen. Bovendien wordt werken met een externe prothese regelmatig als een last ervaren. Zo stijgt de vraag naar reconstructies d.m.v. een interne prothese of d.m.v. lichaamseigen weefsel. Tot slot worden er steeds meer nieuwe technieken ontwikkeld, waardoor het aanbod aan reconstructieve mogelijkheden verder verruimt, met excellente lange termijn resultaten.
Borstsparende heelkunde
Niet elke diagnose van een borsttumor noodzaakt een mastectomie of borstamputatie. Vaak kan een “borstsparende tumorectomie” gebeuren. Hierbij wordt een deel van het klier- en vetweefsel verwijderd. Een aanzienlijke hoeveelheid borstweefsel blijft dus bewaard. Vermits elke plastisch chirurg gedurende zijn of haar opleiding diverse technieken van borstverkleining heeft aangeleerd, kan er in overleg met de borstchirurg een techniek gekozen worden waarbij de tumor zich in het stuk weefsel bevindt dat wordt verwijderd (Fig. 1). Om na de ingreep een grote asymmetrie in de beha te vermijden, kan er geopteerd worden om onmiddellijk of in een tweede tijd een verkleining te laten uitvoeren aan de gezonde zijde. Dit dient uiteraard op voorhand besproken te worden met de patiënte, borstchirurg, oncoloog en plastisch chirurg, en hangt vaak af van het type van tumor.

Fig. 1: Diverse technieken voor borstreductie. Links: superior pedicle. Midden: supero-mediale pedicle. Rechts: inferior pedicle.
Borstreconstructie na een borstamputatie of mastectomie
 Indien er i.k.v. de diagnose van een borsttumor een mastectomie dient te gebeuren, kan een borstreconstructie worden uitgevoerd. Afhankelijk van het type, de grootte van de tumor en de nabehandeling, wordt deze reconstructie onmiddellijk of laattijdig (= reconstructie in een tweede tijd) uitgevoerd.
Indien er i.k.v. de diagnose van een borsttumor een mastectomie dient te gebeuren, kan een borstreconstructie worden uitgevoerd. Afhankelijk van het type, de grootte van de tumor en de nabehandeling, wordt deze reconstructie onmiddellijk of laattijdig (= reconstructie in een tweede tijd) uitgevoerd.
- Een onmiddellijke reconstructie wil zeggen dat er tijdens de ingreep waarbij de borst wordt weggenomen, onmiddellijk een nieuwe borst (of het beginstadium ervan, zie later) wordt gevormd. Niet iedereen komt hiervoor in aanmerking. Dit hangt meestal af van het type en de grootte van de tumor, en of er al dan niet nabehandeling nodig zal zijn. Deze mogelijkheid wordt op voorhand in multidisciplinair teamverband besproken (met de borstchirurg / gynaecoloog, oncoloog, plastisch chirurg, ...)
- Met een laattijdige reconstructie wordt bedoeld dat de borst pas gevormd wordt tijdens een tweede operatie, op latere datum dan de mastectomie-ingreep. Dit is de meest uitgevoerde timing van borstreconstructie. Zo wordt er bijvoorbeeld niet altijd een onmiddellijke reconstructie aangeboden, of kan de reconstructie niet gebeuren in het ziekenhuis waar de borst wordt verwijderd. Soms wil de vrouw eerst het proces van de mastectomie verwerken alvorens aan een reconstructie te denken. Soms wordt een onmiddellijke reconstructie afgeraden omwille van een grote kans op nabehandeling met chemo- en of radiotherapie. Indien er inderdaad een nabehandeling nodig is, en er is geopteerd om pas een reconstructie te laten uitvoeren wanneer deze nabehandeling beëindigd is, zal men steeds een 4- tot 12-tal maanden wachten tot na de beëindiging van de nabehandeling. Op deze mannier kunnen de weefsels en de littekens wat tot rust komen.
Er bestaan diverse types van borstreconstructies. Over het algemeen kunnen ze opgesplitst worden in twee grote groepen:
- Reconstructie met een prothese
- Reconstructie met lichaamseigen weefsel (autoloog weefsel)
1. Reconstructie met een prothese
Een reconstructie met een prothese of een borstimplantaat is mogelijk voor één of beide borsten. Afhankelijk van de wensen van de patiënt, de kwaliteit van de huid en de timing van de reconstructie, onderscheiden we een reconstructie met een prothese in één tijd, versus een reconstructie met een weefselexpander in eerste tijd, gevolgd door een vervangen van de expander door een prothese.
1.1. Reconstructie met enkel een (siliconen-gevulde) prothese
Deze ingreep wordt minder en minder uitgevoerd. Het principe bestaat erin dat het volume borstklier dat verwijderd werd tijdens de mastectomie, vervangen wordt door het volume van een prothese. Deze reconstructie kan bijna alleen maar gebeuren wanneer er een onmiddellijke reconstructie gebeurt. Tijdens dezelfde ingreep wordt het borstweefsel vervangen door een borstprothese die gedeeltelijk onder de grote borstspier wordt geplaatst. Gedeeltelijk, want de onderzijde van de prothese zal enkel bedekt worden door het dunne laagje huid, dat overblijft na de mastectomie. Om deze huid niet te sterk onder druk te zetten, kan het volume van de prothese en dus de nieuwe borst niet te groot zijn.
Als de mastectomie vroeger reeds uitgevoerd werd, is er echter onvoldoende huid aanwezig om deze prothese te bedekken en dient eerst een weefselexpander geplaatst te worden.
1.2. Reconstructie met een expander, nadien gevolgd door een prothese
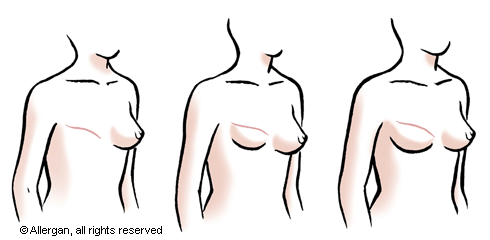
Bij deze procedure, wordt er eerst - i.p.v. een prothese - een expander gedeeltelijk onder de borstpier geplaatst. Deze expander is een soort van ballonnetje dat gradueel de overliggende huid uitrekt en klaarmaakt voor de implantatie van een definitieve prothese (Fig. 2). Na de eerste ingreep waarbij de expander wordt geplaatst, wordt een tweetal weken gewacht tot de littekens goed genezen zijn. Vanaf dat moment wordt de expander elke week opgevuld tijdens een consultatie. Het opvullen gebeurt door de arts of verpleegkundige, en houdt niet meer in dan een prikje dat door de huid wordt gegeven met een naaldje (Fig. 2). Eenmaal de expander het juiste volume heeft bereikt (dat moment is afhankelijk van de grootte van de expander en de grootte van de andere borst), zal een tweede, kleinere ingreep gepland worden (Schema 1). Tijdens deze ingreep, meestal enkele maanden na het plaatsen van de expander, zal de expander vervangen worden door een definitieve siliconen prothese. Deze techniek kan zowel toegepast worden bij een onmiddellijke als een laattijdige reconstructie.
Het plaatsen van een prothese, al dan niet met expander, is een kleine ingreep in vergelijking met een reconstructie met lichaamseigen of autoloog weefsel.
Reconstructies met alleen een prothese en/of expander worden meestal niet voorgesteld bij een onmiddellijke reconstructie wanneer er voor de ingreep al een grote kans bestaat dat er postoperatieve bestraling nodig zal zijn. Een laattijdige reconstructie met een prothese en/of expander zal ook niet worden voorgesteld wanneer er na de mastectomie bestraling is gebeurd. Een dergelijke bestraling heeft immers een zeer slechte invloed op de huid, waarbij deze een “karton-achtig” aspect verkrijgt. De huid rekt dus niet mooi uit, wat de voorwaarde is om deze reconstructie te kunnen uitvoeren. Het risico op wondproblemen wordt zo te groot.
Fig. 2: Reconstructie d.m.v. expander en prothese
Schema 1: Tijdens de mastectomie wordt een expander geplaatst (links). Deze wordt stilaan opgevuld (midden) tot het juiste volume wordt bereikt en dan vervangen door een definitieve prothese (rechts).
2. Reconstructie met lichaamseigen of autoloog weefsel
Een reconstructie met autoloog weefsel wil zeggen dat het weefsel afkomstig is van het lichaam van de vrouw zelf. Er wordt dus geen gebruik gemaakt van een "lichaamsvreemde" prothese. Dit weefsel noemen we een "flap". Hierbij kan geopteerd worden voor reconstructie met een "vrije" of een "gesteelde" flap.
- Een flap is een algemene benaming die gegeven wordt aan een hoeveelheid weefsel met een eigen bloedvoorziening. Het weefsel is dus voorzien van een aanvoerend (slagadertje) en afvoerend bloedvaatje (adertje).
- Bij reconstructies met een vrije flap wordt het weefsel op afstand genomen van de borst (vb. weefsel van de buik met bloedvaatjes in de lies). De bloedvaatjes worden doorgenomen t.h.v. de lies en vervolgens met microchirurgische technieken aan elkaar gekoppeld in de borst.
- Bij een gesteelde flap blijven deze bloedvaatjes verbonden met hun oorspronkelijke locatie (vb. bloedvaatjes in de oksel bij gebruik van de grote rugspier) en dient er dus geen microchirurgie te gebeuren.
2.1. Reconstructie met een gesteelde flap
Reconstructie met de grote rugspier (latissimus dorsi)
Sommige patiënten hebben voldoende vetweefsel op de rug en een relatief kleine borst. Indien men dan de grote rugspier met een bovenliggend huideiland naar voren draait (schema 2), kan dit volume soms genoeg zijn om een even grote borst te bekomen als deze die er was, zonder dat een bijkomende prothese / expander moet geplaatst worden. Vaak is er echter onvoldoende weefsel te vinden op de rug, waardoor er extra volume dient bijgevoegd te worden d.m.v. een prothese of expander.
Wanneer een expander of prothese wordt toegevoegd, is de procedure dezelfde als beschreven in punt 1.1 en 1.2., maar de prothese of expander wordt bijkomend bedekt met de grote rugspier die naar voren wordt gedraaid. Hierdoor kan de volledige prothese/expander (en niet alleen de bovenzijde ervan) bedekt worden met spier en huid. Samen met de spier kan ook een bovenliggend huideiland mee naar voren gebracht worden. Dit is bijvoorbeeld nuttig wanneer er te weinig huid t.h.v. de borst aanwezig is, of wanneer de huid daar bestraald is. De niet-bestraalde huid van de rug kan dan ook met een expander uitgerokken worden tot het gewenste volume. Om de grote rugspier naar voren te kunnen brengen, moet er uiteraard een bijkomend litteken gemaakt worden op de rug. Meestal is dit litteken goed te verbergen onder de bh.
De grote voordelen van deze ingreep zijn de minder zware operatie (kortere operatietijd in vergelijking met een vrije flap, zie verder) en minder kans op mislukking van de ingreep. De nadelen zijn voornamelijk een mogelijk functionaliteitsverlies t.h.v. de schouder (dat meestal niet door de patiënte opgemerkt wordt), het litteken op de rug, en meestal de nood tot bijkomende vulling d.m.v. prothese / expander. Als een expander nodig is, is er dus weer een tweede, kleinere ingreep nodig om de definitieve prothese te plaatsen.
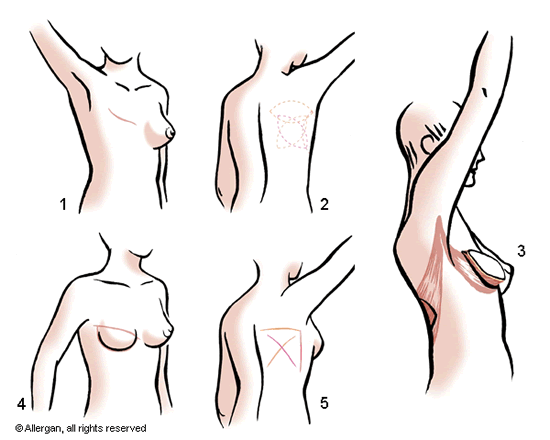
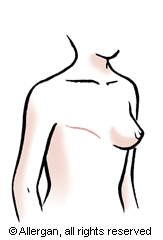
Schema 2: De preoperatieve toestand (1). De diverse aftekeningen die gemaakt kunnen worden om een huideiland naar voren te brengen (2). Het naar voren brengen van de spier met erbovenop een huideiland (3). Het postoperatieve resultaat thv de borst (4). Mogelijke oriëntaties van het litteken t.h.v. de rug (5).
Reconstructie met de buikspier (TRAM-flap)
Hierbij wordt de hoeveelheid vetweefsel en huid van de regio tussen de navel en de schaamstreek samen met de rechte buikspier naar de borst verschoven. Hoewel dit vroeger de standaardbehandeling was voor borstreconstructies, wordt deze techniek meer en meer verlaten omwille van diverse nadelen.
Het belangrijkste nadeel is dat de rechte buikspier wordt weggenomen, wat een sterke verzwakking van de buikwand met zich mee kan brengen. Er bestaan nu technieken waarbij enkel het vetweefsel en de huid van de onderbuik worden overgebracht naar de mastectomie-plaats (zie verder, DIEP- flap). Bovendien heeft men gemerkt dat de betrouwbaarheid van de gesteelde TRAM-techniek minder groot is dan wanneer men een vrije flap zou uitvoeren (zie 2.2.).
2.2. Reconstructie met een vrije flap
Reconstructie met een DIEP-flap van de buik
Wereldwijd is de reconstructie van de borst met een DIEP-flap, d.w.z. met huid- en vetweefsel van de onderbuik, de standaard aan het worden in autologe borstreconstructie (Fig. 3). DIEP staat voor Deep Inferior Epigastric (artery) Perforator, wat de medische benaming is voor het belangrijkste voedende bloedvat van deze flap.
Bij deze techniek worden de bloedvaatjes (adertje en slagadertje) opgezocht die verantwoordelijk zijn voor de bevloeiing van het vetweefsel en de huid tussen de navel en de schaamstreek. Eens deze gevonden en vrijgelegd zijn, worden ze doorgeknipt in de lies en microchirurgisch weer vastgemaakt aan de bloedvaatjes die zich naast het borstbeen bevinden aan de mastectomie zijde. Hierna wordt deze “buikflap’ tot borst gemodelleerd.
Afhankelijk van de hoeveelheid vetweefsel die aanwezig is in de onderbuik, kan deze techniek voor één of beide borsten toegepast worden. Het uiteindelijke volume van de borst is uiteraard afhankelijk van de hoeveelheid vetweefsel die aanwezig is, en kan achteraf in beperkte mate nog bijgesteld worden (zie verder).
De voordelen van deze techniek zijn enorm:
- Er wordt een nieuwe borst gemaakt van enkel eigen weefsel (geen nood voor bijkomende vulling d.m.v. een prothese)
- Het resultaat is levenslang (een prothese moet waarschijnlijk om de 10-15 jaar vervangen worden)
- De borst voelt warm aan
- De borst neemt naar verloop van tijd een zeer natuurlijke vorm aan.
Er zijn echter ook risico’s en nadelen aan verbonden. Vermits er gewerkt wordt met bloedvaatjes die doorgeknipt worden en opnieuw aaneengehecht worden onder de microscoop, bestaat er altijd de kans dat er bloedklontertjes ontstaan in de kleine bloedvaatjes van de flap. Hierdoor verstopt de bloedtoevoer in de flap, waardoor de flap kan afsterven. Dit gebeurt meestal gedurende de eerste 48 uur na de ingreep. Soms kan de flap nog gered worden door de klontertjes operatief te verwijderen. Desalniettemin ligt het percentage op falen van deze techniek op 2 tot 5 %. Bovendien is deze techniek belastend, zowel voor de patiënt (een langere narcose van 5 tot 8 uur), als voor de chirurgen. Het is dan ook bijna onmogelijk om deze techniek toe te passen als er niet in teamverband (twee chirurgen of chirurg met opgeleide assistent) wordt gewerkt. Hoewel deze reconstructie vroeger enkel in universitaire centra werd toegepast (omwille van de moeilijkheidsgraad en omdat daar steeds een “team” voorhanden is), is deze DIEP-flap techniek nu ook mogelijk in grotere niet-universitaire centra zoals het ZOL te Genk, dankzij een goede samenwerking tussen collega’s.

Reconstructie met andere vrije flappen
Wanneer er echter niet voldoende “buikweefsel” voor handen is (bv bij magere patiënten), kan een vergelijkbare techniek gebruikt worden om overtollig weefsel thv de bil (SGAP-flap) of de dij (Gracilis-flap) over te brengen naar de borst.
Bijkomende “correctie”-ingrepen
Bij elk type reconstructie zijn er vaak meerdere kleinere ingrepen nodig na de eerste grotere operatie. Tijdens een tweede fase, de symmetrisatie-fase, wordt de andere (niet geopereerde) borst aangepast aan de gereconstrueerde borst (indien gewenst door de patiënte). Meestal betreft dit een lifting en/of verkleining van de ‘nog niet geopereerde’ borst. Er wordt steeds gestreefd naar een zo groot mogelijke symmetrie in de beha. Het is belangrijk te beseffen dat een perfecte symmetrie zonder beha vaak onmogelijk is.
Hoewel deze tweede fase niet bij iedereen nodig of gewenst is, is de derde fase vaak van groot belang. In deze laatste stap wordt de tepel en het tepelhof gereconstrueerd. De reconstructie van een tepel kan op verschillende manieren gebeuren. Het vaakst wordt er een lokaal flapje gebruikt. Hierbij wordt de aanwezige huid op de borst gebruikt en samengeplooid tot een nieuwe tepel. Na genezing hiervan kan deze getatoeëerd worden samen met het tepelhof. Vermits dit echter specifieke apparatuur en expertise vereist, gebeurt dit in gespecialiseerde centra buiten ons ziekenhuis.
Wanneer en hoe beslist men om een onmiddellijke of laattijdige reconstructie uit te voeren?
- Vaak wordt dit beslist voor de patiënte op basis van het type tumor dat gevonden werd. Vóór de mastectomie wordt uitgevoerd, heeft men immers al een goed idee (aan de hand van afmetingen, biopsies, etc) of er na de ingreep bijkomende behandelingen zullen nodig zijn (radiotherapie en/of chemotherapie). Radiotherapie heeft een zeer slechte invloed op de huid, waardoor deze verstijft en verhardt. Ze wordt “karton-achtig”. Wanneer er zich onder deze huid een prothese of expander bevindt, kan een wonde ontstaan. In minder ernstige gevallen kan zich een sterk littekenweefsel of kapsel vormen rond de expander / prothese, waardoor de borst ernstig misvormd wordt. Ook wanneer er gekozen wordt voor een autologe reconstructie, kan er vetweefsel afsterven (vetnecrose) met vervorming van de reconstructie tot gevolg (zij het in mindere mate). In deze gevallen (wanneer men dus preoperatief weet dat postoperatieve radiotherapie zal nodig zijn) zal er dus eerder voorgesteld worden om een laattijdige reconstructie uit te voeren. Door de radiotherapie zijn de opties voor laattijdige reconstructie verkleind: een reconstructie zonder inbreng van gezond, niet-bestraald weefsel is niet mogelijk. Er moet dus steeds een reconstructie gebeuren met een autologe component (volledig autoloog of autoloog + expander/prothese).
Indien het bijna zeker is dat postoperatief geen radiotherapie zal nodig zijn, dient er overwogen te worden of een onmiddellijke reconstructie haalbaar is. Dit zowel vanuit psychisch als lichamelijk standpunt.
- Lichamelijk: afhankelijk van de gekozen reconstructie zal de periode dat de patiënte in slaap dient te blijven, verlengen. Hierdoor wordt in bepaalde gevallen deze dubbele ingreep (mastectomie + reconstructie) te belastend voor de patiënte.
- Psychisch: niet elke patiënte is klaar om onmiddellijk tot een reconstructie over te gaan. De diagnose van een borsttumor is een mentaal belastende aangelegenheid waarbij de patiënte zo snel mogelijk het gezwel wil laten verwijderen. Vele patiënten zijn dan ook nog niet klaar om al aan een reconstructie te denken. Ze willen eerst de mastectomie verwerken.
Voor deze patiënten bestaat er, zo gewenst, een tussenoplossing: er kan onmiddellijk een tijdelijke expander geplaatst worden, waardoor het maximum van de aanwezige huid kan gespaard blijven bij de mastectomie. Hierdoor heeft de patiënte nog steeds de keuze tussen een laattijdige reconstructie d.m.v. prothese of autoloog weefsel. Indien dan gekozen wordt voor een autologe reconstructie, zal er minder huid van de buik of rug ter plaatse moeten gebracht worden waardoor de reconstructie nog natuurlijker wordt. Indien de patiënte kiest voor het stopzetten van de reconstructie, kan de expander d.m.v. een kleine ingreep verwijderd worden.
- Anderzijds komt het voor dat borstchirurgen de informatie over eventuele reconstructies nog onvoldoende aanreiken aan de patiënte. Hierdoor heeft de patiënte geen weet van het feit dat er een onmiddellijke of laattijdige reconstructie mogelijk is. De reconstructie wordt soms nog aanzien als een soort van ‘luxe-ingreep’ die niet noodzakelijk is. Het tegendeel is echter waar, het aanreiken van informatie over een mogelijke reconstructie, onmiddellijk of laattijdig, kan de patiënte helpen in het verwerkingsproces van de diagnose en initiële behandeling. Het is wetenschappelijk bewezen dat de levenskwaliteit van een vrouw na borstreconstructie drastisch toeneemt.
Belangrijke slotbemerking
Tegenwoordig worden er boeken vol geschreven over allerlei types van borstreconstructies. Met dit korte overzicht hopen wij u de basisinformatie mee te geven. Welke patiënte in aanmerking komt voor welk type van reconstructie, dient individueel besproken te worden met de patiënte, en ook bediscussieerd te worden in multidisciplinair overleg. Belangrijk om weten is dat de mogelijkheid tot borstreconstructie onmiddellijk aan het woord mastectomie zou moeten gekoppeld worden, zoals dit nu al het geval is met bijkomende behandelingen. Borstreconstructies zijn een belangrijk onderdeel in de therapie na een diagnose van borstkanker.
Inhoudsverantwoordelijke:
Dr. Bob Vermeulen, plastische chirurgie - 2018